安奈克替尼获批上市!80%的患者实现肿瘤缩小,ROS1肺癌患者又有新选择!
一、引言
不少肺癌患者常有这样的困惑:为什么EGFR、ALK阳性有那么多药可以选,而ROS1、NTRK等阳性的治疗药物却相对有限?
有不少来自确诊罕见靶点变异患者的“控诉”:“是罕见靶点病人太少了,所以没有药物在研发吗?”
……
尽管罕见靶点阳性的发生率低,但科学家们并未忽视,他们正积极研发创新疗法,旨在为这一群体开辟新的治疗路径。
这不,正值春暖花开之际,携带ROS1变异的肺癌患者也迎来了自己的“春天”!又一新药已经获批上市,为他们的“春天”增添希望之色。

图片说明:安奈克替尼获批报道
二、ROS1变异虽然罕见,但绝非“小众群体”
罕见靶点的概念是相对常见靶点而言的,目前,非小细胞肺癌患者最常见的靶点是EGFR突变[1]。而罕见靶点是指驱动基因发生率低于5%的靶点,包括:ROS1、NTRK、BRAF等[2]。比如:ROS1在我国非小细胞肺癌患者中的变异率为2%-3%[3,4]。
虽然ROS1变异的发生率较低,但由于我国肺癌患者的基数庞大,因此存在ROS1变异的患者实际上也为数不少。ROS1基因有多种变异类型,其中,ROS1融合是主要变异类型。
那么,ROS1变异究竟是怎么一回事?
实际上,ROS1基因位于人体的6号染色体。受外界因素的影响,ROS1基因序列被破坏,这就导致它们给了错的“指令”,使得细胞复制出异常的蛋白质。这些异常的蛋白质随后也会执行异常功能,比如:诱导癌症的发生[5-7]。
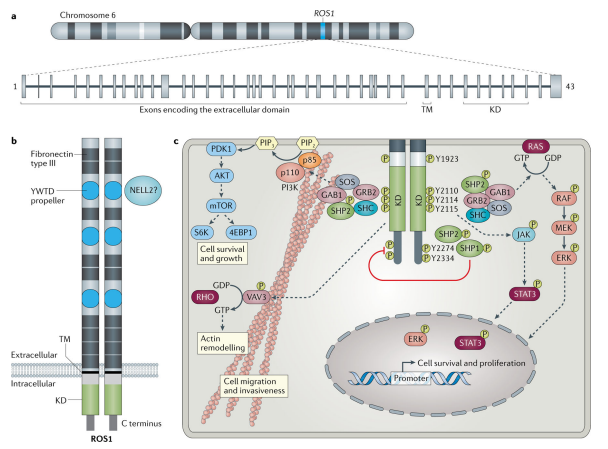
图片说明:ROS1基因位置、蛋白结构、催化诱导的细胞信号通路[7]
而ROS1最常见的融合伴侣为CD74,CD74-ROS1占所有ROS1融合的44%[8]。CD74基因位于5号染色体上,和ROS1基因可以说是“邻居”了。它们频繁“串门”,相互作用,共同促进肿瘤细胞的生存、生长、增殖、迁移和侵袭[7]。
这一密切联动,无疑加剧了问题的严重性!
振奋人心的是,近两年,肺癌领域的新药层出不穷,均为患者们带来了全新的选择。如今,又有一款新药——安奈克替尼,于2024年4月30日正式获批上市,扩宽了ROS1阳性患者的用药思路[9]!
三、好消息:安奈克替尼已获批上市!
我国科学家团队自主研发的安奈克替尼,是一种多靶向(ROS1、ALK、c-MET)的小分子抑制剂,可选择性地抑制ROS1阳性等肿瘤细胞的体外增殖,诱导肿瘤细胞凋亡,起到有效抗癌的作用。
也正是因为独特的作用机制,2023年6月,安奈克替尼用于既往未接受或接受过化疗治疗的ROS1融合阳性晚期NSCLC患者一线治疗的研究结果,在权威医学杂志《Signal Transduction and Targeted Therapy》(影响因子:39.3)上发布[10]。

图片说明:安奈克替尼研究已发布在《Signal Transduction and Targeted Therapy》上[10]
该项研究结果表明,对于整体ROS1阳性患者而言,经安奈克替尼一线治疗后,111例非小细胞肺癌患者中位无进展生存期(mPFS)达到了16.5个月,客观缓解率(ORR)达到了80.2%,其中1例实现完全缓解(CR),88例实现部分缓解(PR)。安奈克替尼80.2%的客观缓解率也意味着,该研究中,80%的患者使用这个药物后,实现肿瘤缩小至少30%且维持6周以上!
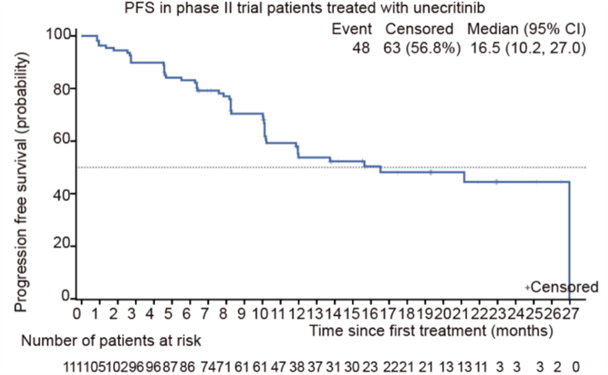
图片说明:安奈克替尼治疗总人群的PFS[10]
不仅如此,安奈克替尼也较好地满足了CD74-ROS1融合肺癌患者的生存需求。
我们在前文提到,ROS1融合阳性的非小细胞肺癌患者中,有44%的患者携带CD74-ROS1融合。与其他类型ROS1融合患者相比,携带CD74-ROS1融合的患者,无进展生存期明显更短,更易发生脑转移,预后更差[11-13]。如今,他们也等来了新的治疗选择。
该项研究表明,对于CD74-ROS1融合患者,经安奈克替尼一线治疗后,27例非小细胞肺癌患者mPFS达到了21.2个月,ORR达到了88.9%,其中1例实现CR,23例实现PR。值得强调的是,该研究中,近89%的CD74-ROS1融合患者使用安奈克替尼后,实现肿瘤缩小至少30%且维持6周以上!比起整体ROS1阳性人群,ORR有了进一步的提升!
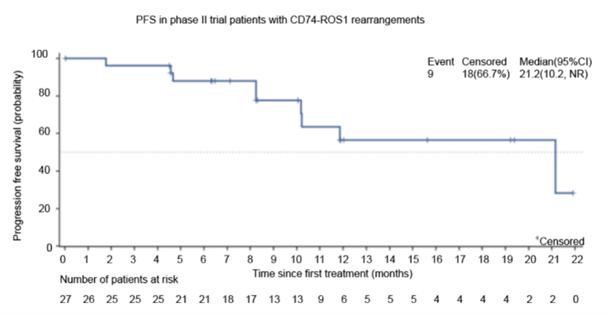
图片说明:安奈克替尼治疗CD74-ROS1融合患者的PFS[10]
不仅如此,研究进一步证明,经安奈克替尼治疗后,33例基线发生脑转移患者mPFS达到了10.1个月,ORR达到了72.7%。该研究中,近73%的脑转移患者使用安奈克替尼后,实现肿瘤缩小至少30%且维持6周以上。
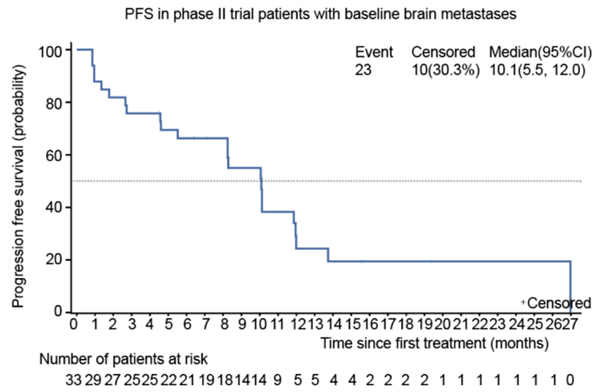
图片说明:安奈克替尼治疗基线脑转移ROS1阳性患者的PFS[10]
以上数据均由独立评审委员会评估
如今,安奈克替尼开始崭露头角,其疗效潜力也引人关注,有望为更多ROS1阳性(尤其是CD74-ROS1阳性)的晚期非小细胞肺癌患者,带来新的治疗选择!
四、ROS1阳性患者长期用药有保障
俗话说“是药三分毒”。随着靶向治疗逐渐成为ROS1阳性患者的一线治疗推荐,许多患者也开始担心持续用药问题,担心副作用影响药物疗效和患者生活质量。
那么,安奈克替尼是否会带来更多的“安全隐患”?
实际上,安奈克替尼实现持久缓解的同时,安全且可耐受[10]!
I/II期研究中证明,安奈克替尼治疗后不良事件大多为1-2级,3级及以上发生率低。值得强调的是,相较于其他ROS1靶向药,安奈克替尼导致的神经毒性和眼部毒性发生率低,且无3级或更高级别的神经毒性和眼部毒性发生。
总而言之,安奈克替尼治疗相关不良事件可以通过减量或暂停用药及对症支持治疗控制,无治疗相关的死亡发生。
五、展望
生命无价。而对于晚期罕见靶点阳性的肺癌患者而言,一线治疗决策尤为关键。此时,精准选择合适的治疗方案至关重要。
如今,多靶点抑制剂——安奈克替尼的出现,为ROS1阳性的晚期肺癌患者开辟了新的治疗“通道”,更让那些因担忧“副作用”而对靶向治疗踌躇不前的患者,拥有了选择靶向治疗的信心与可能。
我们翘首以盼,期待安奈克替尼能够为晚期ROS1阳性患者带来更多获益,更多希望!
参考文献
1、侯占胜,张宴魁,江波. EGFR-TKI联合治疗在晚期非小细胞肺癌中的研究进展. 中国医学创新,2023,20(10):174-179.
2、房雪,曲春静,白元松,代恩勇. NGS法检测197例非小细胞肺癌突变基因特征分析. 中国实验诊断学,2022,26(2):261-264.
3、Kohno T, Nakaoku T, Tsuta K, et al. Beyond ALK-RET, ROS1 and other oncogene fusions in lung cancer. Transl Lung Cancer Res. 2015;4(2):156-164.
4、Zhang Q, Wu C, Ding W, et al. Prevalence of ROS1 fusion in Chinese patients with non-small cell lung cancer. Thorac Cancer. 2019;10(1):47-53.
5、Lin JJ, Shaw AT. Recent Advances in Targeting ROS1 in Lung Cancer. J Thorac Oncol. 2017;12(11):1611-1625.
6、江薇. ROS1融合基因突变在非小细胞肺癌诊断与治疗中的研究进展. 中国肿瘤临床,2019,46(5):257-262.
7、Drilon A, Jenkins C, Iyer S, Schoenfeld A, Keddy C, Davare MA. ROS1-dependent cancers - biology, diagnostics and therapeutics. Nat Rev Clin Oncol. 2021;18(1):35-55.
8、Lu S, Pan H, Wu L, et al. Efficacy, safety and pharmacokinetics of Unecritinib (TQ-B3101) for patients with ROS1 positive advanced non-small cell lung cancer: a Phase I/II Trial. Signal Transduct Target Ther. 2023;8(1):249.
9、NMPA官网获批
10、Lu S, Pan H, Wu L, et al. Efficacy, safety and pharmacokinetics of Unecritinib (TQ-B3101) for patients with ROS1 positive advanced non-small cell lung cancer: a Phase I/II Trial. Signal Transduct Target Ther. 2023;8(1):249.
11、Gendarme S, Bylicki O, Chouaid C, Guisier F. ROS-1 Fusions in Non-Small-Cell Lung Cancer: Evidence to Date. Curr Oncol. 2022;29(2):641-658.
12、Li Z, Shen L, Ding D, et al. Efficacy of Crizotinib among Different Types of ROS1 Fusion Partners in Patients with ROS1-Rearranged Non-Small Cell Lung Cancer. J Thorac Oncol. 2018;13(7):987-995.
13、Zhang Y, Zhang X, Zhang R, et al. Clinical and molecular factors that impact the efficacy of first-line crizotinib in ROS1-rearranged non-small-cell lung cancer: a large multicenter retrospective study. BMC Med. 2021;19(1):206.



